Nadzieja dla rodziców – nowy lek na Zespół Angelmana!
 Dwie firmy farmaceutyczne: Ovid Therapeutics i Lundbeck A/S zawarły umowę licencyjną na lek o nazwie: Gaboxadol (OV101). Firma Ovid zamierza wykorzystać go w oddzielnych badaniach klinicznych w leczeniu Zespołu Angelmana (ang. Angelman Syndrome, AS) i Zespołu Łamliwego chromosomu X (ang. Fragile X Syndrome).
Dwie firmy farmaceutyczne: Ovid Therapeutics i Lundbeck A/S zawarły umowę licencyjną na lek o nazwie: Gaboxadol (OV101). Firma Ovid zamierza wykorzystać go w oddzielnych badaniach klinicznych w leczeniu Zespołu Angelmana (ang. Angelman Syndrome, AS) i Zespołu Łamliwego chromosomu X (ang. Fragile X Syndrome).
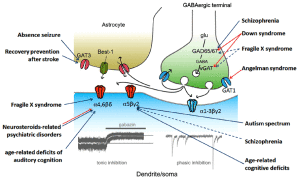
Gaboxadol jest wysoko selektywnym synaptycznym receptorem GABA(A), który przywraca „tonic inhibition”. Na modelu mysim AS wykazano poprawę niedoboru motorycznego. Gaboxadol zwiększa poziom transportera GABA1 (GAT1) w obserwowanym mysim modelu. Planowane jest wprowadzenie leku do 2 fazy badań klinicznych w 2016 roku.
Dr Matthew During, prezydent i dyrektor naukowy firmy Ovid Therapeutics stwierdził: „Dla firmy Ovid to wielki zaszczyt i przywilej pracować ze społecznością Angelmana. Słowa i wyrazy nadziei i zainteresowania naszą pracą jest niezwykle satysfakcjonujące. Nasze wsparcie FAST i ASF przekroczyło nasze oczekiwania. Z niecierpliwością oczekujemy na wprowadzenie OV101 do badań klinicznych i mamy nadzieję, że lek ten spowoduje znaczącą różnicę w życiu pacjentów z Zespołem Angelmana jak również ich rodzin.”
Dan Harvey, prezes Naukowego Komitetu Doradczego ASF (Angelman Syndrome Fundation) powiedział: „Gaboxadol ma potencjał w leczeniu objawów Zespołu Angelmana w różnych grupach wiekowych, nie tylko u małych dzieci. Podejście do leczenia przy użyciu leku Gaboxadol symptomów choroby związanych z padaczką, zdolnościami motorycznymi i poznawczymi jest odmienne od innych leków i metod badawczych.”
FAST (Foundation for Angelman Syndrome Therapeutics) i ASF (Angelman Syndrome Foundation) ogłoszą społeczności związanej z Zespołem Angelmana kiedy rozpocznie się rekrutacja dzieci do prób klinicznych.
Poniżej informacja prasowa firmy Ovid.
Ovid planuje rozpoczęcie 2 fazy badań klinicznych w 2016 roku.
Kopenhaga i Nowy Jork, 16.04.2015r
H. Lundbeck A/S – globalna firma farmaceutyczna specjalizująca się w chorobach mózgu oraz prywatna firma Ovid Theraupeutics, spółka farmaceutyczna skupiająca się na opracowaniu terapii rzadkich i osieroconych chorób mózgu, poinformowały, że w dniu 25.03.2015r podpisały umowę licencyjną na wyłączność na Gaboxadol, który jest pierwszym doustnym lekiem posiadającym możliwość leczenia pacjentów z Zespołem Angelmana i Zespołem Łamliwego Chromosomu X. Gaboxadol (OV101) jest małą cząsteczką, wysoko selektywnym synaptycznym receptorem GABA(A), który był już testowany w badaniach klinicznych.
Zgodnie z warunkami umowy, Ovid uzyskuje wyłączne prawo na rozwój i komercjalizację leku OV101 na całym świecie. Firma Lundbeck jako mniejszościowy udziałowiec Ovid, otrzyma środki pieniężne ze sprzedaży należności licencyjnych. Ovid jest odpowiedzialny za wszelki przyszły rozwój i komercjalizację OV101. Dodatkowe warunki finansowe nie zostały ujawnione.
Anders Gersel Pedersen, wiceprezes i szef Działu Badań i Rozwoju firmy Lundbeck oświadczył: „Jesteśmy bardzo zadowoleni z tej umowy umożliwiającej rozwój leku Gaboxadol jako potencjalnego leczenia dla pacjentów, którzy nie mają obecnie żadnych dostępnych możliwości medycznych. Jeśli osiągniemy sukces, to ten program rozwoju leku może zmienić życie tych pacjentów.”
OV101 jest obecnie testowany w 1 fazie badaniach klinicznych. Poprzez przywrócenie w niskich dawkach tzw. „tonic inbibition” daje obiecujące funkcjonalne ulepszenie w modelach Zespołu Angelmana i Zespołu Kruchego Chromosomu X jak również w genetycznym modelu epilepsji.
„Dokładnie w 50 rocznicę pierwszego opisania choroby Zespołu Angelmana przez brytyjskiego pediatrę Harrego Angelmana (1915-1996) jesteśmy na drodze rozwoju nowego leku. Istnieje pilna potrzeba terapii, która dotyczy rzadkich chorób neurologicznych jakich jak Zespoł Angelmana i Zespół Kruchego Chromosomu X.” powiedział dr Matthew During.
Firma Ovid uważa, że dowody kliniczne i przedkliniczne leku Gaboxadol, wskazują na hamowanie zaburzeń padaczkowych i zwiększenie funkcji ruchowych i poznawczych. Lek OV101, w 1 fazie badań klinicznych prowadzonych na 3000 pacjentów, był dobrze tolerowany.
Źródło:
http://www.angelman.org/news/upcoming-angelman-syndrome-clinical-trial/
http://journal.frontiersin.org/article/10.3389/fncir.2013.00170/full
Dodaj komentarz
Musisz się zalogować, aby móc dodać komentarz.