Regulacja enzymu CaMKII przy użyciu inżynerii genetycznej
 Doktor Edwin Weeber, który jest aktualnie profesorem na Uniwersytecie Południowej Florydy (ang. University of South Florida – USF) poświęcił swoją karierę naukową by prowadzić studia (badania) nad Zespołem Angelmana (ZA). Po dziesięciu latach badań i testów, odkrył on w jaki sposób można cofnąć deficyty choroby Zespołu Angelmana u myszy. Przed badaniami Weebera większość poszukiwań, jakie były prowadzone w kierunku ZA były badaniami genetycznymi. W 1997 roku został odkryty gen (UBE3A), który prowadzi do zaburzeń Zespołu Angelmana.
Doktor Edwin Weeber, który jest aktualnie profesorem na Uniwersytecie Południowej Florydy (ang. University of South Florida – USF) poświęcił swoją karierę naukową by prowadzić studia (badania) nad Zespołem Angelmana (ZA). Po dziesięciu latach badań i testów, odkrył on w jaki sposób można cofnąć deficyty choroby Zespołu Angelmana u myszy. Przed badaniami Weebera większość poszukiwań, jakie były prowadzone w kierunku ZA były badaniami genetycznymi. W 1997 roku został odkryty gen (UBE3A), który prowadzi do zaburzeń Zespołu Angelmana.
„Nieprawidłowości w działaniu tego genu, jak uważano, były odpowiedzialne za chorobę ZA. UBE3A podlega napiętnowaniu w mózgu, co znaczy, że organizm wie które geny są odziedziczone od matki, a które od ojca. Delecja (ubytek-brak) lub mutacja tego genu, pochodzącego od matki powoduje ZA” – mówi Weeber. Doktor Weeber będąc zainteresowany biomedycznymi aspektami ZA, rozpoczął badanie enzymów i białek, które regulowane są przez ten gen w mózgu. Odkrył, że potrafi cofnąć efekty ZA poprzez odpowiednią regulację głównego enzymu – „CaMKII, który bierze zasadniczy udział w procesie uczenia się i pamięci, a także w nauce umiejętności motorycznych. Odkryliśmy, że jedną z biologicznych nieprawidłowości myszy z ZA jest redukcja aktywności CaMKII. Wiadomo już było, że ograniczenie aktywności CaMKII powoduje deficyty neurologiczne. Tak więc stwierdziliśmy, że uregulowanie aktywności tego enzymu, może cofnąć deficyty neurologiczne u myszy,” – mówi Weeber.
Gdy doktor Weeber przetestował swą teorię poprzez skrzyżowanie myszy ZA z myszami z mutacją (z zachowaniem prawidłowej regulacji aktywności CaMKII), okazało się, że u potomstwa ZA nie wystąpił. Drgawki padaczkowe, upośledzenie umysłowe, i problemy z koordynacją ruchową – wszystko to zniknęło u modelowych myszy. Wyniki te doprowadziły Weebera do wniosku, że delecja lub mutacja matczynej części genu UBE3A powoduje obniżenie aktywności enzymu CaMKII, co skutkuje zespołem Angelmana. Weeber twierdzi, że regulacja aktywności enzymu CaMKII prowadzi do korekty działania matczynej części genu UBE3A. Weeber dodaje, że enzym ten nie jest produkowany zanim mysz się urodzi. Tak może być również u ludzi. Weeber mówi, że ten wniosek jest ważny ze względu na leczenie ZA. „To sugeruje, że ZA nie ma charakteru rozwojowego, lecz raczej biochemiczny. Innymi słowy połączenia neuronów mózgowych wydają się być prawidłowe, lecz to zmiana aktywności CaMKII uniemożliwia prawidłową komunikację pomiędzy neuronami w obszarach mózgu, gdzie występuje matczyne piętnowanie genu UBE3A.”
Doktor Weeber wraz rodziną przeprowadził się na Florydę, gdzie na miejscowym uniwersytecie objął profesurę, gdyż uczelnia ta znana jest z badań poznawczych. Tam Weeber będzie kontynuował praktykę terapeutyczną z pacjentami z ZA.Wyniki badań Weebera na myszach zostały uzyskane za pomocą inżynierii genetycznej, więc ta metoda nie ma zastosowania u ludzi. Twierdzi on jednak, że jedną z metod leczenia ZA u ludzi mogłoby być leczenie farmakologiczne mogące modulować CaMKII. Inna metoda może polegać na wykorzystaniu wirusa AAV (adeno-associated virus). Weeber wyjaśnia, że jest to metoda polegająca na wprowadzaniu obcych genów w neuronach w ośrodkowym układzie nerwowym. AAV mógłby być użyty do wprowadzenia CaMKII z tej samej mutacji, która została wykorzystana w celu ratowania myszy ZA, lub do wprowadzenia genu UBE3A, który mogłyby zająć miejsce delecji lub mutacji matczynego genu UBE3A. Weeber planuje zbadanie możliwości użycia wirusa AAV w leczeniu ZA w najbliższych sześciu miesiącach. Rodzice dzieci z ZA bardzo mocno doceniają dotychczasową pracę doktora Weebera.
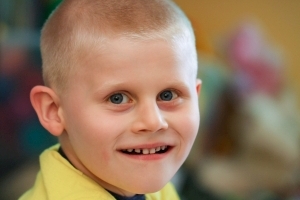
Dzieci z syndromem Angelmana często się śmieją i uśmiechają ale ta radosna postawa maskuje poważne problemy neurologiczne – opóźnienie umysłowe, problemy z poruszaniem się oraz ataki drgawek.
Jednak nowe badania na myszach sugerują, że wiele z tych niedoborów może być zaspokojonych (załagodzonych).
Dr Edwin Weber i jego współpracownicy odwrócili niedobory neurologiczne w modelu myszy z syndromem Angelmana poprzez uniemożliwienie zahamowania CAMKII, czyli enzymu silnie przyspieszonego w strefach mózgu dotkniętych Syndromem Angelmana.
Wyniki, które zostały przedstawione w marcowym wydaniu Nature Neuroscience (obecnie dostępnym online) ukazują istotną część mechanizmu określającego warunek i punkt do potencjalnych celów terapeutycznych do leczenia tych symptomów. Syndrom Angelmana, który dotyka 1 na 15.000 dzieci to dolegliwość osłabiająca układ neurologiczny, która charakteryzuje się opóźnieniem umysłowym, drastycznie (znacznie) ograniczoną mową oraz problemami z poruszaniem się i utrzymaniem równowagi.
W 1997 roku naukowcy odkryli, że syndrom Angelmana występuje z powodu mutacji pojedynczego genu, nazwanego UBE3A. Następnie odkryli oni modelową mysz syndromu Angelmana na której były prowadzone prace na zmutowanym genie. Odkrycie to było kłopotliwe, stwierdził Weber, gdyż UBE3A to gen „ housekeeping”, co oznacza, że reguluje on na szeroką skalę procesy zachodzące w komórkach, nie koniecznie specyficzne dla jakiegokolwiek z niedoborów neurologicznych występujących u chorych dzieci. Swoiście, białko zakodowane przez UBE3A „Tags” (zwiąże) inne białka z degradacją w „koszu” komórkowym, proteasom.
„Najtrudniejszą rzeczą do racjonalizacji( usprawnienia) jest to, że gen „housekeeping” po którym nikt się nie spodziewał, że może mieć jakikolwiek wpływ – powoduje ciężkie opóźnienie umysłowe”, powiedział Weber. „tak więc postanowiliśmy spróbować zidentyfikować część obiektów molekularnych białek”
W tym procesie, Weber i jego współpracownicy zidentyfikowali anormalność w modelu myszy z syndromem Angelmana – zmiany w enzymie zwanym- CaMK II ( Calcium/calmodulin – Dependent Protein Kinase II), który jest ważny w procesie komórkowym, który tkwi u podstaw procesu zapamiętywania i nauki.
Odkryli oni, że w syndromie Angelmana, aktywność CaMKII została zredukowana w związku z zahamowaniem/hamującą zmianą chemiczna (phosphorylation). W związku z widoczną rolą CaMK II w czynnościach neurologicznych, Weber podejrzewał, że to może tłumaczyć ( odpowiadać za) niedobory zaobserwowane u dzieci z syndromem Angelmana. Przez przypadek, jeden ze współpracowników Webera – dr Ype Elgersma z Centrum Medycznego Erasmus w Rotterdamie w Holandii – stworzył mysz z mutacją, która zapobiega zahamowaniu CaMK II. Naukowcy zadecydowali, aby hodować myszy Angelmana z myszami o zmutowanym CaMK II, aby zaobserwować czy neutralizacja (przeciwdziałanie) zahamowaniu CaMK II załagodzi problemy neurologiczne.
Następnie naukowcy otrzymali „podwójne mutanty” poprzez „bartery” testów neurologicznych oraz poznawczych.
Myszy Angelmana osiągały słabe wyniki w zadaniach z nauki i zapamiętywania i przejawiały osłabioną koordynację ruchową.
„Podwójne mutanty” natomiast okazywały normalne zdolności nauki i zapamiętywania oraz koordynację ruchową. Również podczas gdy myszy Angelmana miały skłonności do napadów drgawek, podwójne mutanty okazywały bardzo niską skłonność do nich.
Weber był zaskoczony tak rozrosłymi osiągnięciami. „Myśleliśmy, że być może odkryjemy pewne z niedoborów, które zaobserwowaliśmy u modelowych myszy” – powiedział Weber.” Nie mieliśmy pojęcia, że uda się nam odkryć właściwie wszystko”.
Pomimo, iż zastosowanie inżynierii genetycznej zastosowanej w powyższym badaniu nie jest możliwe do zastosowania u ludzi Weber uważa, że odkrycia te mogą okazać się punktem zwrotnym do określania nowych celów w terapii tej dolegliwości.
Jednakże wyniki te mogą zostać zastosowane znacznie szerzej, powiedział Weber, do innych typów syndromów opóźnienia umysłowego, które pozostają niewyjaśnione i nieuleczalne.
„Istnieje wiele syndromów opóźnienia umysłowego, których nadal nie rozumiemy. Być może zmiany w CaMKII utożsamiane z syndromem Angelmana mogłyby być zastosowana również w innych syndromach opóźnienia.”
Źródło:
http://free4web.pl/3/2,135190,378208,6516030,Thread.html
https://www.cureangelman.org/news/longshot.html
http://weeberlab.com/labmem.html
Dodaj komentarz
Musisz się zalogować, aby móc dodać komentarz.